Pesquisa é realizada pelo Hemocentro de Ribeirão em parceria com o Butantan; coordenador do Nutera traz os detalhes
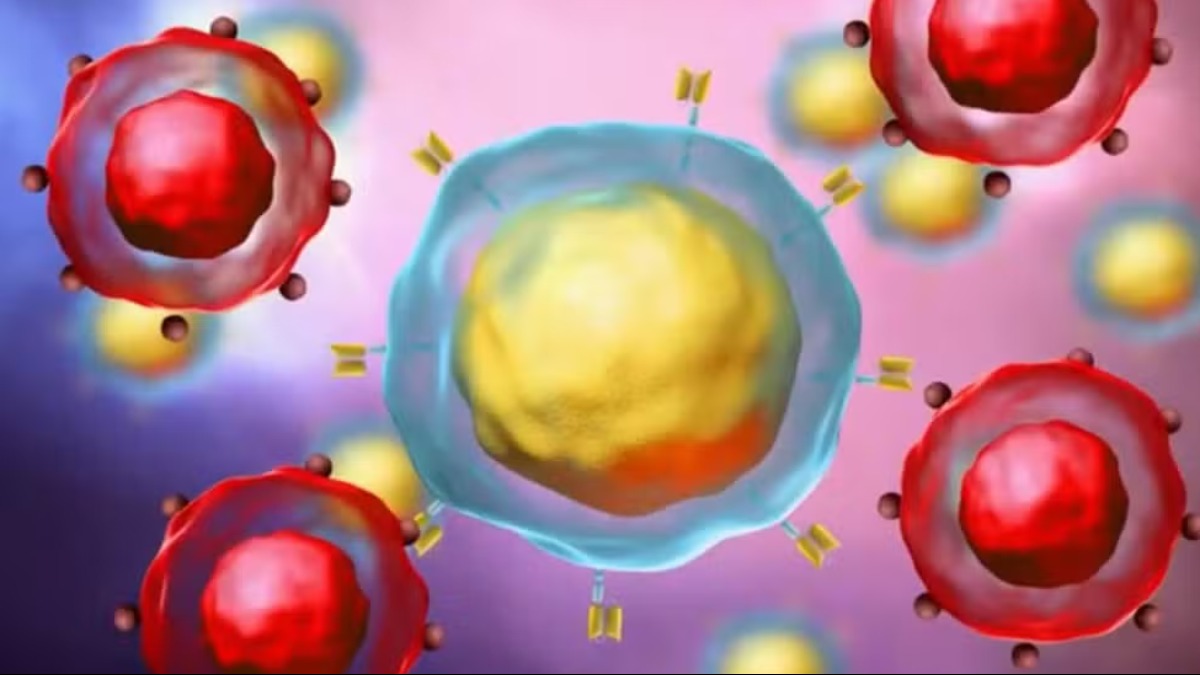
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou a segunda fase do estudo clínico do Cart-Hydra, terapia celular produzida em parceria entre o Hemocentro de Ribeirão Preto e o Instituto Butantã. A primeira fase, focada na segurança do tratamento, mostrou resultados positivos, permitindo a progressão para a próxima etapa.
Segurança e Efetividade do Cart-Hydra
O estudo clínico, coordenado pelo professor doutor Diego Villaclé, comprovou a segurança do Cart-Hydra na primeira fase. Os pacientes tratados apresentaram um perfil de segurança excelente, sem eventos adversos graves. A Anvisa, satisfeita com os resultados, autorizou a expansão do estudo para incluir mais pacientes e hospitais.
Expansão do Estudo Clínico
Com a aprovação da Anvisa, a segunda fase do estudo clínico irá expandir para quatro novos hospitais – três em São Paulo e um em Campinas. Serão tratados mais pacientes com leucemia e linfoma, totalizando 81 participantes até 2025. Os resultados desta fase serão cruciais para comprovar a efetividade do tratamento além da segurança já demonstrada.
Leia também
Disponibilização do Cart-Hydra no SUS
O objetivo final é disponibilizar o Cart-Hydra no Sistema Único de Saúde (SUS), expandindo o acesso a essa terapia inovadora para pacientes em todo o Brasil. A equipe espera solicitar o registro do tratamento junto à Anvisa em 2026, após a conclusão da segunda fase do estudo. A disponibilização do Cart-Hydra no SUS representaria um avanço significativo no tratamento de leucemia e linfoma, oferecendo esperança de cura para muitos pacientes que não dispõem de outras opções.